Моль как найти: Молярная масса — что это? Как рассчитать? Формулы и примеры
Молярная масса — что это? Как рассчитать? Формулы и примеры
Что такое моль
Прежде чем говорить о том, как найти молярную массу вещества, определимся с понятием «моль». Его ввели как искусственную величину для упрощения расчетов. Это количество вещества, в котором содержится столько же мельчайших частиц, сколько в 12 г одного из изотопов углерода — C12.
Для всех химических веществ это количество одинаково и представляет собой число Авогадро 6,02 · 1023. Постоянная Авогадро обозначается NA, а измеряется в моль-1.
Число Авогадро — это количество молекул, ионов или других мельчайших частиц в 1 моле вещества.
NA = 6,02 · 1023 моль-1.
Историческая справка
В 1811 году химик Амедео Авогадро предположил, что если взять два равных объема газов в равных значимых условиях (при одинаковой температуре и давлении), то количество молекул в этих объемах тоже будет одинаковым. Опираясь на свою гипотезу, он определил атомные и молекулярные массы многих веществ, а также рассчитал количество атомов в молекулах воды, оксидов азота и т. д. Однако в научных кругах гипотеза Авогадро долго не находила понимания. Общепринятой она стала только в 1860 году.
Опираясь на свою гипотезу, он определил атомные и молекулярные массы многих веществ, а также рассчитал количество атомов в молекулах воды, оксидов азота и т. д. Однако в научных кругах гипотеза Авогадро долго не находила понимания. Общепринятой она стала только в 1860 году.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Что такое молярная масса
Молярная масса — это масса одного моля вещества, она измеряется в граммах деленных на моль (г/моль). Данная величина представляет собой отношение массы вещества к его количеству, которое измеряется в молях.
Как обозначается молярная масса: М.
, где — это масса вещества, а — количество вещества.
Единица измерения молярной массы: г/моль.
Запоминаем!
Правильно говорить именно молярная, а не мольная масса.
Несмотря на то, что в 1 моле любого химического вещества содержится одинаковое количество молекул (и оно равно числу Авогадро), молярные массы разных веществ отличаются. Все потому, что отличаются атомы, которые входят в состав этих молекул. В частности, разница между ними заключается в относительной атомной массе (Ar) — например, Ar(Mg) = 24, а Ar(Hg) = 200. Сейчас станет ясно, какое это имеет значение.
Как определить молярную массу
Данная величина тесно связана с такими понятиями, как относительные атомная и молекулярная массы. Именно относительные, потому что абсолютную массу молекулы или атома вещества в химии не используют для решения задач — это слишком малые величины.
Относительная атомная масса вещества (Ar) показывает, во сколько раз его атом больше 1/12 атома углерода. Это значение для каждого химического элемента можно увидеть в таблице Менделеева.
Относительная молекулярная масса (Mr) складывается из Ar каждого атома в молекуле вещества с учетом индексов. Она показывает, на сколько масса молекулы больше 1/12 атома углерода.
, где — это количество атомов.
Разберемся на примерах.
В молекуле хлорида натрия NaCl есть 1 атом натрия и 1 атом хлора, при этом Ar(Na) = 23, Ar (Cl) = 35,5.
Mr(NaCl) = 23 + 35,5 = 58,5.
В молекуле NaNO2 есть 1 атом натрия, 1 атом азота и 2 атома кислорода.
Ar(Na) = 23, Ar(N) = 14, Ar(O) = 16.
Mr(NaNO2) = 23 + 14 + 16 · 2 = 69.
Собственно, для вычисления молярной массы больше ничего и не требуется.
Важно
Молярная масса вещества численно равна относительной молекулярной массе. Но путать эти два понятия не стоит — у них разный физический смысл. Молярная масса характеризует 1 моль, а относительная молекулярная — 1 молекулу.
Но путать эти два понятия не стоит — у них разный физический смысл. Молярная масса характеризует 1 моль, а относительная молекулярная — 1 молекулу.
Количество вещества
Из предыдущих формул понятно, что молярная масса и количество вещества тесно связаны. Рассмотрим эту связь подробнее. Начнем с того, что количество вещества может обозначаться как латинской буквой , так и греческой буквой (ню). Международное обозначение — , но не стоит удивляться, встретив в формулах любую из этих букв.В формуле нахождения молярной массы мы обозначили количество вещества через :
, следовательно .
Пользуясь этим, можно найти количество вещества (в молях), если нам известны его абсолютная и молярная масса.
Пример 1
Как определить, какое количество вещества включают 350 г сульфата бария BaSO4?
Воспользуемся формулой .
Мы помним, что M = Mr (значение молярной массы равно значению относительной молекулярной).
Mr(BaSO4) = Ar(Ba) + Ar(S) + Ar(O) · 4 = 137 + 32 + 16 · 4 = 233.
М(BaSO4) = Mr(BaSO4) = 233 г/моль.
Подставим значение молярной массы в формулу:
моль.
Есть и еще одна формула количества вещества, которая позволяет найти его, если известно число молекул или других структурных единиц.
, где — число структурных единиц, — число Авогадро.
Пример 2
Допустим, некий объем CaCO3 содержит 3,01 · 1023 молекул. Как найти количество вещества, соответствующее данному объему?
Воспользуемся формулой моль.
Молярный объем
Выше мы находили количество вещества через молярную массу, но для газов это можно сделать и через молярный объем. Согласно закону Авогадро количество любого газа, равное 1 моль, будет занимать один и тот же объем, если газы рассматриваются при одинаковой температуре и давлении.
При стандартных физических условиях — температуре 0°С и давлении 1 атм или 760 мм ртутного столба, 1 моль газа занимает объем 22,4 л.
Молярный объем — это объем газа, взятого в количестве 1 моль. Он обозначается Vm.
При нормальных условиях Vm = 22,4 л/моль.
Значения молярного и фактического объема газа помогают найти количество вещества.
, где — фактический объем газа, а — молярный объем.
Пример 1
Сколько молей содержится в 120 литрах газа при нормальных условиях?
Рассчитаем по формуле моль.
Относительная плотность одного газа по другому
Иногда для решения задачи нужно знать, как найти молярную массу газа, о котором сообщается лишь его плотность по воздуху или по другому газу.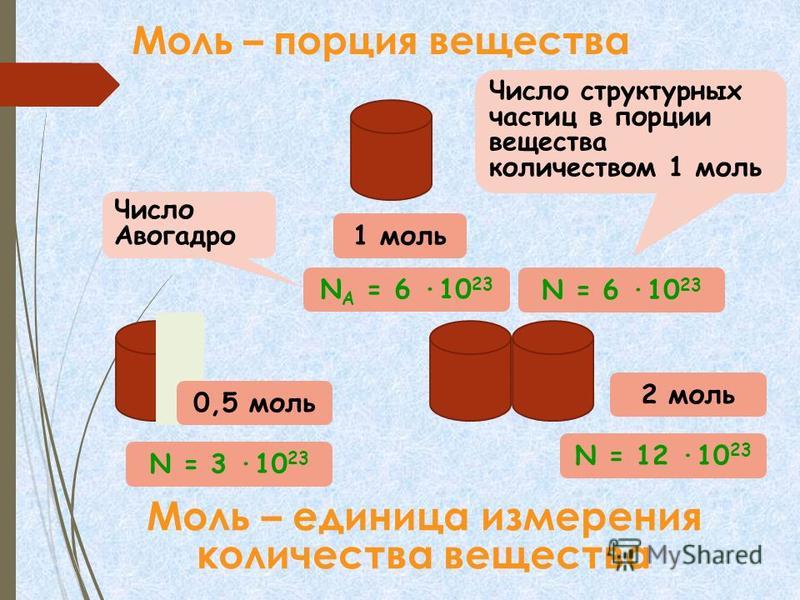 Это возможно, если знать формулу относительной плотности, которая обозначается буквой D.
Это возможно, если знать формулу относительной плотности, которая обозначается буквой D.
, где и — некие газы.
Пример 1
Как определить, во сколько раз угарный газ плотнее водорода?
Для начала найдем молярную массу CO и H2:
М(CO) = Mr(CO) = Ar(C) + Ar(O) = 12 + 16 = 28.
М(H) = Mr(H2) = 2 · Ar(H) = 2 · 1 = 2.
.
Ответ: угарный газ в 14 раз плотнее водорода.
Пример 2
Как посчитать молярную массу газа х, о котором известно, что он в 10 раз плотнее углекислого газа CO2?
Подсчитаем для начала молярную массу углекислого газа:
M(CO2) = Mr(CO2) = 12 + 2 · 16 = 44.
Ориентируясь на формулу относительной плотности, произведем расчет молярной массы искомого газа х.
М(х) = D(х/CO2) · M(CO2) = 10 · 44 = 440 г/моль.
Ответ: у данного газа молярная масса 440 г/моль.
Примеры задач
Итак, мы разобрались, как находить молярную массу жидкости, газа или твердого тела и как это понятие связано с количеством вещества, а также с относительной плотностью одного газа по другому. Чтобы закрепить знания, посмотрите, как эти сведения применяются в решении задач.
Задача 1
Известно, что 300 г неустановленного вещества содержат 12,04 · 1023 молекул. Чему равна молярная масса данного вещества?
Дано:
N(х) = 12,04 · 1023.
m(х) = 300 г.
M(х) = ?
Решение:
Найдем количество вещества моль.
Подставим количество вещества в формулу :
г/моль.
Ответ: молярная масса данного вещества 150 г/моль.
Задача 2
Какой объем займет водород в количестве 0,7 моль?
Дано:
моль.
Решение:
По формуле мы можем найти объем .
Зная, что молярный объем при обычных условиях составляет 22,4 л/моль, вычислим фактический объем водорода:
л.
Ответ: объем водорода составляет 15,68 литров.
Задача 3
В порции оксида серы SO3 содержится 8,356 · 1023 атомов кислорода. Какова масса этой порции?
Дано:
N(O) = 8,356 · 1023.
m(SO3) = ?
Решение:
Для решения задачи нам подходит формула , т. е. . Но для начала нужно найти количество вещества.
Мы знаем, что в одной молекуле SO3 есть 3 атома кислорода, исходя из этого можно вычислить количество молекул в порции оксида:
, следовательно .
Зная количество молекул, рассчитаем количество вещества:
моль.
Теперь можно узнать молярную массу SO
M(SO3) = 32 + 16 · 3 = 80 г/моль.
Рассчитаем фактическую массу через молярную массу:
г.
Ответ: абсолютная масса порции оксида серы 36,8 грамм.
Задача 4
Как рассчитать молярную массу простого вещества, о котором известно, что в порции 100 г содержится 15,05 · 1023 молекул? Назовите это вещество.
Дано:
m(x) = 100 г.
N(x) = 15,05 · 1023.
М(х) = ?
Решение:
В данном случае поможет вычислить молярную массу NA, с помощью которого мы сначала узнаем количество вещества:
моль.
Исходя из этого, рассчитаем молярную массу:
г/моль.
Ответ: согласно таблице Менделеева можно предположить, что это кальций Ca.
Задача 5
Определите, насколько сероводород H2S плотнее водорода H2?
Решение:
Нам требуется вычислить относительную плотность сероводорода по водороду:
.
Для этого вычислим молярные массы H2S и H2:
М(H2S) = 1 · 2 + 32 = 34 г/моль.
М(H2) = 1 · 2 = 2 г/моль.
Подставим значения в формулу:
.
Ответ: сероводород в 17 раз плотнее водорода.
Вопросы для самопроверки
Что такое число Авогадро и чему оно равно?
В чем измеряется молярная масса?
Напишите формулу молярной массы вещества.

Какая формула связывает количество вещества и его объем?
Как узнать количество вещества, если известно число молекул в порции?
2.2. Моль, молярная масса
2.2. Моль, молярная масса2.2. Моль, молярная масса
В химических процессах участвуют мельчайшие частицы – молекулы, атомы, ионы, электроны. Число таких частиц даже в малой порции вещества очень велико. Поэтому, чтобы избежать математических операций с большими числами, для характеристики количества вещества, участвующего в химической реакции, используется специальная единица – моль.
Моль — это такое количество вещества, в котором содержится определенное число частиц (молекул, атомов, ионов), равное постоянной Авогадро
Постоянная Авогадро NA определяется как число атомов, содержащееся в 12 г изотопа 12С:
Таким образом, 1 моль вещества содержит 6,02 • 1023 частиц этого вещества.
Исходя из этого, любое количество вещества можно выразить определенным числом молей ν (ню). Например, в образце вещества содержится 12,04 • 1023 молекул. Следовательно, количество вещества в этом образце составляет:
В общем виде:
где N – число частиц данного вещества;NA – число частиц, которое содержит 1 моль вещества (постоянная Авогадро).
Молярная масса вещества (M) – масса, которую имеет 1 моль данного вещества.
Эта величина, равная отношению массы m вещества к количеству вещества ν, имеет размерность кг/моль или г/моль. Молярная масса, выраженная в г/моль, численно равна относительной относительной молекулярной массе Mr (для веществ атомного строения – относительной атомной массе Ar).
Например, молярная масса метана CH4 определяется следующим образом:
 е. 16 г CH4 содержат 6,02 • 1023 молекул.
е. 16 г CH4 содержат 6,02 • 1023 молекул.Молярную массу вещества можно вычислить, если известны его масса m и количество (число молей) ν, по формуле:
Необходимо отметить, что значение молярной массы вещества определяется его качественным и количественным составом, т.е. зависит от Mr и Ar. Поэтому разные вещества при одинаковом количестве молей имеют различные массы m.
Пример
Вычислить массы метана CH4 и этана С2H6,
взятых в количестве ν = 2 моль каждого.
Молярная масса метана M(CH4) равна 16 г/моль;
молярная масса этана M(С2Н6) = 2 • 12+6=30 г/моль.

Отсюда: m(CH4) = 2 моль • 16 г/моль = 32 г;
m(С2Н6) = 2 моль • 30 г/моль = 60 г.
Таким образом, моль – это порция вещества, содержащая одно и то же число частиц, но имеющая разную массу для разных веществ, т.к. частицы вещества (атомы и молекулы) не одинаковы по массе.
n(CH4) = n(С2Н6), но m(CH4) (С2Н6)
Вычисление ν используется практически в каждой расчетной задаче.
Калькулятор крота
Создано Jack Bowater
Отзыв от Bogna Szyk и Steven Wooding
Последнее обновление: 16 декабря 2022 г.
Содержание:- Что такое крот?
- Как рассчитать моли – конвертер молей в граммы
- Часто задаваемые вопросы
Хотите узнать, как рассчитать моли? Нужен калькулятор граммов в моли или даже калькулятор молей в граммы? Что ж, тогда вы пришли в нужное место.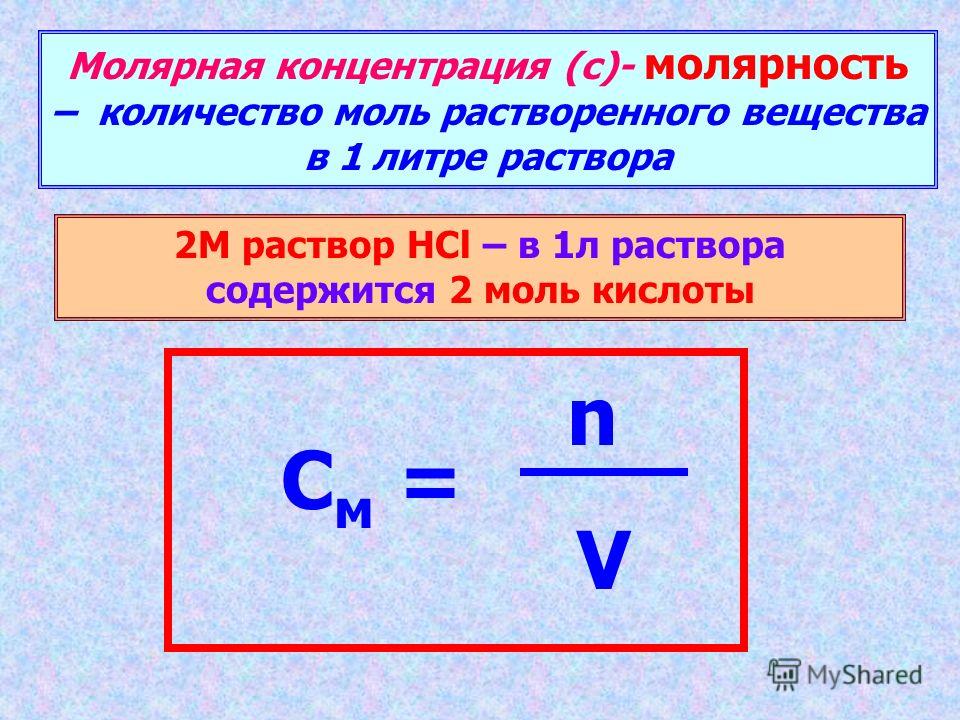 С нашим конвертером молей в граммы вы можете легко конвертировать между массой, молекулярной массой и молями . Химия стала немного проще! Удивите своих друзей своей поразительной способностью определять, сколько у вас молей вещества в килограммах, унциях или даже тоннах! (Также полезно для любых серьезных промышленных приложений, для всех вас, инженеров-химиков.)
С нашим конвертером молей в граммы вы можете легко конвертировать между массой, молекулярной массой и молями . Химия стала немного проще! Удивите своих друзей своей поразительной способностью определять, сколько у вас молей вещества в килограммах, унциях или даже тоннах! (Также полезно для любых серьезных промышленных приложений, для всех вас, инженеров-химиков.)
Пока мы говорим о химии, у нас есть несколько других калькуляторов, которые могут вам пригодиться. Почему бы не проверить наш калькулятор молярности или наш калькулятор процентного выхода?
Что такое родинка?
Крот — это маленькое подземное млекопитающее, принадлежащее к семейству Talpidae. Шучу — мы уверены, что вы никогда раньше не слышали эту шутку. Моль — это то, как химики определяют количество вещества, полезное при работе с множеством различных молекул, реагирующих одновременно (т. Е. Любая реакция). Официальное определение Международной системы единиц гласит, что моль — это количество химического вещества, которое содержит ровно 6,02214076×10 23 (постоянная Авогадро) атомов, молекул, ионов или электронов (составных частиц) , по состоянию на 20 го мая 2019 года. До этого моль определялся как количество атомов в 12 граммах углерода-12 (изотопа углерода). Оказывается, запоминать это определение для моего экзамена по химии GCSE было бессмысленно. Стыд.
До этого моль определялся как количество атомов в 12 граммах углерода-12 (изотопа углерода). Оказывается, запоминать это определение для моего экзамена по химии GCSE было бессмысленно. Стыд.
Итак, почему химики используют кроты и зачем нужен калькулятор кротов? Что ж, как мы уже говорили выше, это полезная метрика при работе с реакциями. Может быть, пример объяснит это лучше всего. Допустим, вы хотите нейтрализовать 10 г соляной кислоты (HCl в воде) небольшим количеством гидроксида натрия (NaOH). Теперь вы хотите, чтобы полученный раствор был совершенно нейтральным, поэтому вы не хотите добавлять слишком много или слишком мало NaOH, делая его слишком щелочным или кислым соответственно. Поэтому полезно выяснить, сколько именно молекул HCl содержится в растворе. Вот тут и пригодятся родинки.
Чтобы узнать, как рассчитать количество молей, используйте уравнение:
моль = масса / молекулярная масса
Если вы хотите найти концентрацию соляной кислоты, вы можете использовать наш калькулятор концентрации.
Как рассчитать моли – конвертер молей в граммы
Давайте рассмотрим быстрый пример, который поможет объяснить, как конвертировать моли в граммы или граммы в моли. Мы знаем, что у нас есть 10 г HCl с молекулярной массой 36,5 г/моль. Подставим эти числа в приведенное выше уравнение:
моль = 10 / 36,5 = 0,27 моль = 1,626×10²³ молекул HCl
Мы можем определить количество молекул, умножив количество молей на приведенную выше постоянную Авогадро. Теперь мы знаем количество молекул HCl, которое у нас есть, и, поскольку реакция 1:1, , нам нужно точно такое же количество молекул NaOH, чтобы нейтрализовать ее . Поскольку нам нужно найти массу добавляемого NaOH, давайте быстро перестроим уравнение:
моль = масса / молекулярная масса (умножьте обе части на молекулярную массу),
моль × молекулярная масса = масса (перестройте уравнение),
масса = молекулярная масса × моль .
Поскольку 1,626×10 23 молекул NaOH также равно 0,27 моля, а мы знаем, что молекулярная масса NaOH равна 40, мы можем использовать эти числа, чтобы получить:
масса = 40 × 0,27 = 10,8 г
Итак, теперь мы знаем, что нам нужно 10,8 г NaOH , чтобы точно нейтрализовать наше количество соляной кислоты.
Мы надеемся, что этот калькулятор преобразования граммов в моли (или калькулятор молей в граммы) поможет вам в химических расчетах! Вам также может пригодиться наш калькулятор титрования.
Часто задаваемые вопросы
Что такое родинка?
Один моль равен количеству вещества, которое содержит ровно 6,022×10 23 чего-то . Хотя это что-то может быть чем угодно, поскольку это такое большое число, оно обычно зарезервировано для атомов, молекул, электронов и ионов.
Как найти молярную массу?
Чтобы найти молярную массу:
- Найдите химическую формулу рассматриваемого соединения.

- Возьмите периодическую таблицу.
- Найдите атомную массу каждого атома.
- Сложите атомную массу каждого атома.
- Результатом будет молярная масса вашего вещества .
Как найти количество молей вещества?
Для расчета количества молей вещества:
- Измерьте вес вашего вещества.
- Используйте периодическую таблицу , чтобы найти его атомную или молекулярную массу.
- Разделить вес на атомную или молекулярную массу.
- Проверьте свои результаты с помощью Omni Calculator.
Как преобразовать граммы в моли?
Чтобы преобразовать граммы в моли:
- Найдите периодическую таблицу.
- Рассчитайте атомную или молекулярную массу вашего вещества.
- Разделить вес на атомную или молекулярную массу.

- Используйте Omni Calculator, чтобы проверить свой ответ.
Сколько граммов в моле?
Количество граммов в моле зависит от вещества , которое у вас есть. Чтобы вычислить это, найдите атомную или молекулярную массу вашего вещества и умножьте на количество имеющихся у вас молей. Для одного моля атомная или молекулярная масса будет равна весу .
Сколько атомов в моле?
В моле 6,02214076×10 23 атомов. Он получен из числа атомов в 12 г изотопа углерода-12.
Джек Боуотер
Молекулярный вес
г / моль
Ознакомьтесь с 11 похожими калькуляторами стехиометрии Инфографика
Предоставьте своим ученикам инструменты, которые помогут им справиться с любыми трудностями, связанными с кротами и числом Авогадро
Источник: © Дэн Брайт0018 . Это число ( 6,02 x 10 23 ) происходит от количества атомов в 12 г углерода-12 (это изотоп углерода с шестью протонами и шестью нейтронами).
Итак, мы можем сказать, что один моль протонов имеет массу один грамм, а один моль нейтронов имеет массу один грамм, так как протоны и нейтроны имеют одинаковые массы.
Это означает, что:
- Один моль из 1 атомов Н имеет массу один г.
- Один моль из 19 атомов F имеет массу 19 г, а два моля имеют массу 38 г.
- Один моль молекул NH 3 , имеющий относительную молекулярную массу ( Mr ) 17, имеет массу 17 г, а половина моль имеет массу 8,5 г.
- Один моль ибупрофена (C 13 H 18 O 2 ) имеет массу 206 г, а 0,01 моль имеют массу 2,06 г (что все же намного больше, чем в ибупрофене). планшет).
Моли позволяют нам сравнивать количество атомов или молекул в двух или более разных веществах без записи длинных чисел.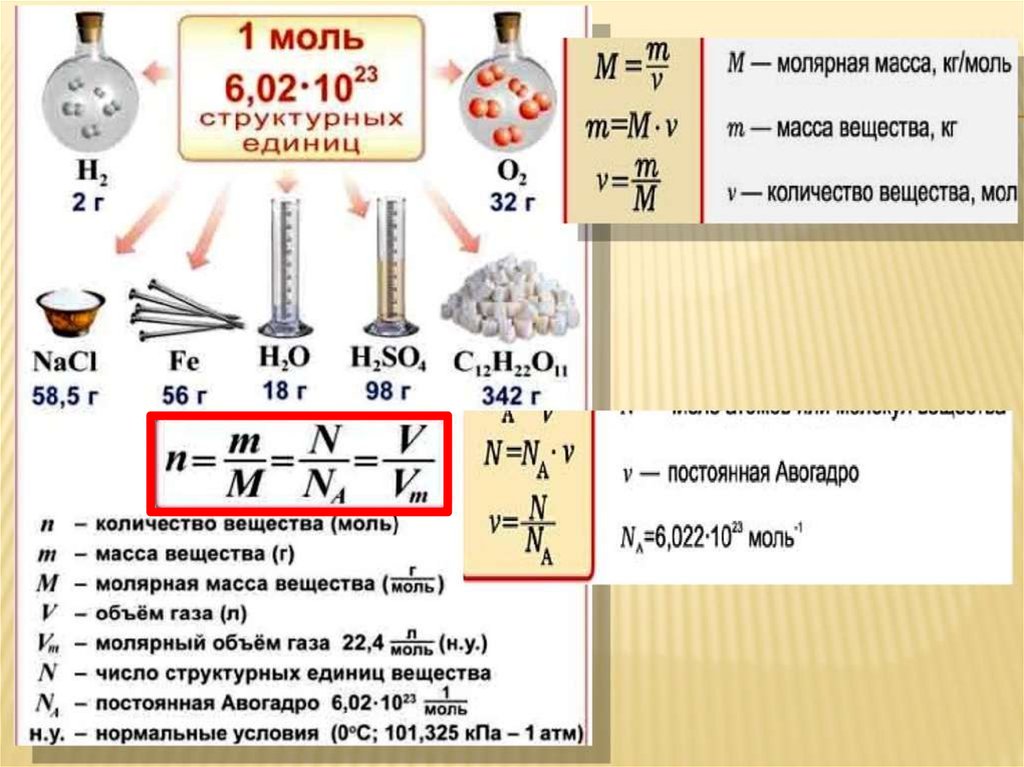
Загрузите этот
Инфографический плакат, информационный бюллетень, рабочий лист и заметки для учителя. Покажите плакат в классе или на проекторе. Кроме того, распечатайте его и используйте в качестве раздаточного материала.
Используйте прилагаемый информационный бюллетень и рабочий лист, чтобы ваши учащиеся могли применить свои математические навыки к трем различным типам задач, связанных с родинками.
- Плакат в формате pdf (или плакат на белом фоне в формате pdf)
- Информационный бюллетень в формате MS Word или pdf
- Заметки учителя и ответы в формате MS Word или pdf
- Рабочий лист для учащихся в формате MS Word или pdf
СКАЧАТЬ ВСЕ
Вычисление молей
Связь между молями (моль), массой (г) и Mr (г моль -1 ) можно представить следующим уравнением:
Знаете ли вы?
Средний пушистый европейский крот весит примерно 100 г. Итак, кротов из пушистых европейских кротов будут иметь массу: 6,02 х 10 22 кг. Аналогичен массе Луны в 7,35 х 10 22 кг. Это один огромный клубок меха.
Аналогичен массе Луны в 7,35 х 10 22 кг. Это один огромный клубок меха.
Постоянная Авогадро
Помните, что мы говорили, что моль — это действительно большое число …
Мы можем использовать постоянную Авогадро для расчета числа атомов или молекул из числа молей или наоборот, используя следующее соотношение :
Знаете ли вы…?Амедео Авогадро не рассчитал значение молей , но он был первым, кто заявил, что разные газы при одинаковом объеме и давлении будут содержать одинаковое количество частиц. К сожалению, он умер до того, как кто-либо вычислил число, которое носит его имя.
Дополнительные ресурсы
- Используйте идеи, изложенные в этих пяти шагах, чтобы помочь учащимся освоить расчеты молей.
- Викторина для учащихся 16–18 лет по молям, молям и массам и другим химическим методам с этими вопросами количественной химии.



